Weitere Methoden der Keimidentifizierung
Biochemische Methoden (u. a. API-Systeme)
Die Anwendung miniaturisierter biochemischer Systeme gehört zum Standard eines mikrobiologischen Labors. Voraussetzung für eine richtige Identifizierung ist das Vorliegen einer Reinkultur sowie die vorherige Bestimmung kultureller Merkmale (Gram-Verhalten, Katalase-Test, Oxidase-Test, Sporenbildungsvermögen, mikroskopisches Bild).
Das ifp nutzt z. B. die sogenannten API-Identifizierungssysteme (Analytical Profile Index), die relevante Gruppen von Bakterien und Hefen abdecken. Es wird die Verwertbarkeit von bestimmten Kohlenhydraten oder die Bildung spezifischer Stoffwechselprodukte bestimmt, deren Auswertung ein numerisches Profil ergibt, das über einen Datenbankenabgleich zum Identifizierungsergebnis führt. In Abhängigkeit von dem verwendeten System vergehen bis zum Vorliegen des Ergebnisses 4 - 72 Stunden.
Sequenzierung (16S- bzw. 18S- oder ITS-rDNA)
Diese molekularbiologische Methode der Identifizierung beruht auf der Vervielfältigung eines spezifischen und hochvariablen Bereichs der ribosomalen DNA (rDNA) von Mikroorganismen mittels PCR (Polymerase-Kettenreaktion) und der nachfolgenden Sequenzierung des Amplifikats.
Dazu sind folgende Arbeitsschritte notwendig:
- Isolierung der genomischen DNA aus Bakterien, Hefen oder Schimmelpilzen (Reinkultur)
- Durchführung der PCR: 16S-rDNA (Bakterien) bzw. 18S- oder ITS-rDNA (Hefen und Schimmelpilze)
- Aufreinigung des PCR-Produktes
- Sequenzierung des PCR-Produktes
- Auswertung der Sequenz über z. B. NCBI BLAST
Das Ergebnis der molekularbiologischen Identifizierung liegt nach ca. 3 Tagen vor.
Kulturelle Methoden (Schimmelpilze)
Die klassische Identifizierung von Schimmelpilzen beruht auf der makroskopischen und mikroskopischen Untersuchung von Reinkulturen auf geeigneten Nährmedien. Die charakteristischen morphologischen Merkmale der Kolonien sowie des mikroskopischen Bildes werden mit Literaturdaten verglichen.
Keimidentifizierung mittels MALDI-TOF-Massenspektrometrie
Mit der MALDI-TOF-Massenspektrometrie (Matrix Assisted Laser Desorption lonization - Time of Flight) hat das ifp im Bereich der Mikrobiologie eine moderne Methode zur Keimidentifizierung etabliert.
Keimidentifizierung anhand des spezifischen ribosomalen Proteinspektrums
Die Identifizierung mittels MALDI-TOF basiert darauf, dass jeder zu bestimmende Mikroorganismus einen einzigartigen molekularen Fingerabdruck besitzt. Dieser besteht aus einem für den jeweiligen Mikroorganismus ganz speziellen Proteinspektrum. Um dieses zu erhalten werden gezielt die ribosomalen Proteine, die in allen Mikroorganismen in großen Mengen zu finden sind, analysiert. Durch den Abgleich der charakteristischen Spektren dieser Proteine mit mehreren Datenbanken wird ein zu bestimmender Mikroorganismus eindeutig identifiziert.
Ionisierung und Nachweis im Flugzeit-Detektor
Dazu wird von einer Reinkultur ausgehend der zu bestimmende Mikroorganismus entweder direkt oder nach einer kurzen Proteinextraktion auf einen Probenträger aufgebracht, mit einer organischen Matrix überschichtet mit dem MALDI-TOF massenspektrometrisch vermessen. Das Messprinzip beruht darauf, dass das Analyt-Matrix-Gemisch mit einem Laser beschossen und damit ionisiert wird. Die Ionen werden durch ein Flugrohr geleitet und ihre einzelnen Massen detektiert. Es resultiert das spezifische Massenspektrum, mit dem der zu bestimmende Mikroorganismus identifiziert wird. Die Messung dauert nur wenige Minuten.
Die Vorteile der Identifizierung von Mikroorganismen mittels MALDI-TOF
- Schnelligkeit und Präzision
- kleinster Bedarf an Probenmengen
- Identifizierung von Bakterien, Hefen und Schimmelpilzen
- Erweiterung der Datenbank
- Aufbau kundenspezifischer Datenbanken
- Speicherung aller Spektren und Auswertungen
- Sicherung der Rückverfolgbarkeit bei Kontaminationen
Keimidentifizierung
Eine schnelle und sichere Identifizierung von Keimen ist in vielen Bereichen der Produktion von Lebensmitteln, Kosmetika oder Pharmaka bzw. im Rahmen von Hygieneuntersuchungen die Voraussetzung für eine sachkundige Bewertung und Beherrschung von Kontaminationen. Das ifp Institut für Produktqualität bietet folgende Möglichkeiten zur Identifizierung von Mikroorganismen an:
- MALDI-TOF (Massenspektrometrie)
- biochemische Methoden (API-Systeme)
- Sequenzierung (16S- bzw. 18S- oder ITS-rDNA)
- kulturelle Methoden (klassische Mikrobiologie)
Die Identifizierung erfolgt an Proben wie:
- Isolaten, Rein- und Mischkulturen auf festen Medien oder in flüssigen Anreicherungen
- Medien aus dem Monitoring wie Kontaktplatten, Luftkeimzahlplatten, Slides
- Platten aus Ansätzen zur Bestimmung der Keimzahl
Die Isolierung von Mikroorganismen zur nachfolgenden Identifizierung kann aus nahezu allen Proben von Lebensmitteln bis zu den Bedarfsgegenständen erfolgen. Die Voraussetzung für die Identifizierung ist das Vorliegen einer Reinkultur, die über den Schritt der Subkultivierung auf einem geeigneten Medium hergestellt wird.
Konservierung von Mikroorganismen
Das ifp Institut für Produktqualität bietet die Langzeitaufbewahrung von identifizierten Isolaten an, die dem Kunden als zusätzliche Teststämme oder Hauskeime für Prüf- und Validierungsarbeiten oder Vergleichszwecke zu späteren Zeitpunkten zur Verfügung stehen.
Pharmawasser - Wasser zur pharmazeutischen Verwendung
Auf Grund der besonderen Stellung von aufbereitetem Wasser in der pharmazeutischen Industrie als Produktbestandteil oder als Wasser im Produktionsgebrauch sind die Qualitätsvorgaben für diesen wichtigsten Rohstoff besonders hoch.
Im Europäischen Arzneibuch (Ph. Eur.) sind in den Monographien zu den Wasserqualitäten die Reinheitskriterien definiert (Monographien nach Ph. Eur., in aktueller Fassung).
- Gereinigtes Wasser (Aqua purificata) ist für die Herstellung von Arzneimitteln bestimmt, die weder steril noch pyrogenfrei sein müssen, unterschieden in „Gereinigtes Wasser als Bulk“ und „In Behältnisse abgefülltes gereinigtes Wasser“.
- Hochgereinigtes Wasser (Aqua valde purificata) ist für die Herstellung von Arzneimitteln vorgesehen, für die Wasser von hoher biologischer Qualität benötigt wird.
- Wasser für Injektionszwecke (Aqua ad iniectabilia) ist Wasser, das zur Herstellung von Arzneimitteln zur parenteralen Anwendung bestimmt ist, deren Lösungsmittel Wasser ist, unterschieden in „Wasser für Injektionszwecke als Bulk“ und „Sterilisiertes Wasser für Injektionszwecke“.
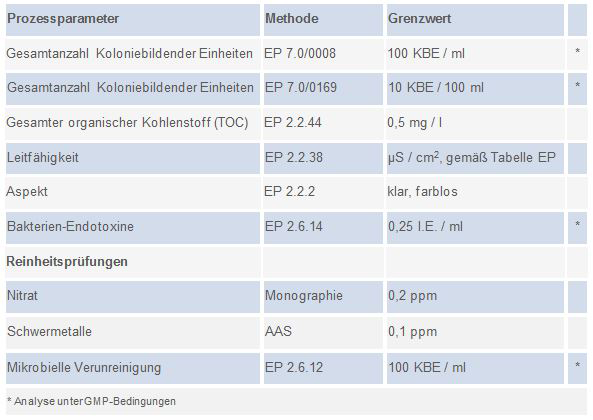
Das ifp Institut für Produktqualität bietet die für die Qualitätsüberprüfung nach Ph. Eur. anzuwendenden Verfahren wie nachfolgend beschrieben an (klicken Sie auf das Bild, um die Liste der Verfahren anzusehen):
Mikrobiologische Prüfung von Arzneimitteln
In der pharmazeutischen Industrie spielen mikrobiologische Nachweise eine bedeutende Rolle, da sie meist von den ersten Schritten der Produktentwicklung bis zur endgültigen Freigabe durch die Qualitätssicherung involviert sind. Hierbei wird u. a. die Sterilität eines Produktes oder auf die Abwesenheit pathogener Keime, die Auslöser von Infektionen sein können, kontrolliert. Zusätzlich muss sichergestellt werden, dass eine mikrobiologische Belastung von Pharmazeutika nur unterhalb definierter Grenzwerten auftritt.
Mikrobiologischer Service für Hersteller von Arzneimitteln und pharmazeutischen Rohstoffen
- Prüfungen auf mikrobielle Reinheit
- Validierung der Prüfung auf mikrobielle Reinheit
- Prüfung auf Sterilität
- Validierung der Prüfung auf Sterilität
- Prüfung auf ausreichende antimikrobielle Konservierung
- Prüfungen auf Bakterien-Endotoxine
- Validierung der Prüfung auf Bakterien-Endotoxine
- Untersuchungen von Wasser für pharmazeutische Zwecke
- Durchführung von Eignungsprüfungen an Nährmedien (Growth Promotion Test)
- Untersuchungen von Monitoring-Proben
- Untersuchung von Bioindikatoren
- Identifizierung von Mikroorganismen